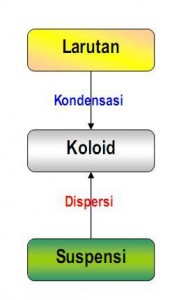
Oleh karena ukuran partikel koloid berada pada rentang antara larutan sejati dan suspensi kasar, maka sistem koloid dapat diperoleh melalui dua cara, yakni: pemecahan partikel-partikel besar menjadi parikel berukuran koloid. Cara ini disebut cara dispersi. Pembentukan agregat dari molekul-molekul kecil pembentuk larutan menjadi ukuran koloid. Cara ini disebut sebagai cara kondensasi.
Cara dispersi
Beberapa metode praktis yang bisa digunakan untuk membuat koloid dan tergolong cara dispersi secara sederhana adalah istilah terkait dengan cara mekanik, cara peptisasi, homogenisasi, dan cara busur listrik Bredig.
Cara mekanik
Menurut cara ini, zat yang akan didispersikan dalam medium pendispersi digiling sampai ukurannya berada pada rentang partikel-partikel koloid. Dengan demikian, partikel zat terdispersi diperkecil hingga ukuran koloid.
Contoh cara ini misalnya penggilingan kacang kedelai pada pembuatan tahu, pembuatan cat di industri menggunakan cara ini, dimana bahan untuk membuat cat digiling sampai berukuran koloid kemudian didispersikan ke dalam medium pendispersi seperti air, atau terpentin.
Cara busur listrik
Pada cara busur listrik Bredig, arus listrik bertegangan tinggi dialirkan melalui dua buah elektroda logam sebagai bahan terdispersi dicelupkan ke dalam air hingga dua ujung elektroda itu nyaris bersentuhan. Loncatan bunga api listrik menimbulkan bahan elektroda menguap dan larut di dalam medium pendispersi seperti air membentuk sol. Logam-logam yang didapat dalam membentuk sol dengan cara ini secara sederhana adalah istilah terkait dengan platina, emas, perak.
Cara peptisasi
Dispersi koloid dapat juga diperoleh dari suspensi dengan cara memecahkan partikel-partikel dari suspensi kasar. Kemudian menambahkan ion-ion yang dapat diadsorpsi oleh partikel-partikel koloid hingga koloid tersebut menjadi stabil.
Dalam prakteknya, kedalam suspensi kasar ditambahkan larutan ion sejenis kemudian dilakukan pengadukan. Adanya pengadukan ini menimbulkan agregat endapan terpecah menjadi agregat-agregat yang lebih kecil menuju ukuran koloid. Koagulasi agregat-agregat yang telah membentuk ukuran koloid dapat dihambat karena adanya ion-ion yang teradsorpsi. Cara seperti ini dikenal sebagai cara peptisasi.
Cara homogenitas
Pembuatan koloid jenis emulsi tertentu dapat dilakukan dengan menggunakan mesin penghomogen atau mesin untuk membuat zat menjadi homogen dan berukuran koloid. Cara ini digunakan pada pembuatan susu.
Partikel lemak dari susu diperkecil sampai berukuran koloid dengan cara melewatkan zat tersebut melalui lubang berpori dengan tekanan tinggi. Bila ukuran partikel telah sesuai maka zat tersebut didispersikan ke dalam medium pendispersinya.
Cara kondensasi
Menurut cara ini, ion-ion atau molekul yang berukuran sangat kecil (biasanya membentuk larutan sejati bila di larutkan kedalam air) diperbesar menjadi partikel-partikel sebesar ukuran koloid. Dengan kata lain, terlarut sejati diubah menjadi dispersi koloid. Cara kondensasi umumnya dilakukan melalui reaksi kimia. Tiga macam reaksi yang dapat menghasilkan kondensasi secara sederhana adalah istilah terkait dengan reaksi hidrolisis, reaksi redoks, dan reaksi metatesis.
Reaksi metatesis
Apabila kedalam larutan natrium tiosulfat ditambahkan larutan asam klorida akan terbentuk partikel berukuran koloid. Persamaan kimianya adalah:
Na2S2O3 + 2HCl ® 2NaCl + H2SO3 + S
Terbentuknya partikel berukuran koloid karena belerang yang terbentuk akan beragregat yang semakin lama semakin besar sampai berukuran koloid. Bila konsentrasi pereaksi dan suhu reaksi tidak dikendalikan, dispersi koloid tidak akan terbentuk, sebab partikel belerang akan tumbuh terus menjadi endapan yang tidak larut dalam air.
Reaksi redoks
Sol emas melalui reduksi emas(III) klorida dengan formalin. Persamaan kimianya:
AuCl3 + CH4O + 3H2O ® 2Au + 6HCl + CH4O2
Emas pertama-tama akan terbentuk dalam keadaan atom-atom bebasnya, kemudian terbentuk agregat yang lebih besar menjadi berukuran partikel koloid, dan distabilkan oleh adanya ion-ion OH– yang teradsorpsi pada permukaan partikel koloid, ion-ion OH– ini berasal dari air yang terurai.
Reaksi hidrolisis
Besi(III) klorida yang berwarna coklat tua bila dilarutkan kedalam air akan menguraikan air membentuk ion OH– dan ion OH+. Ion-ion OH– bereaksi dengan besi(III) klorida membentu besi(III) hidroksida. Persamaan kimianya:
FeCl3 + 3H2O ® Fe(OH)3 + HCl
Ukuran partikel-partikel Fe(OH)3 yang terbentuk lebih besar dari ukuran larutan sejati tetapi tidak cukup besar untuk mengendap. Selain itu, koloid yang terbentuk distabilkan dengan mengadsorpsi ion-ion Fe3+.
Pengubahan medium pendispersi
Kondensasi dapat terjadi bila kelarutan zat dikurangi dengan cara mengganti pelarutnya. Contoh, jika larutan belerang jenuh dalam etanol dituangkan kedalam air, maka akan terbentuk sol belerang karena terjadi penurunan kelarutan belerang dalam pelarut capuran air dan etanol.
Pembentukan larutan koloid dengan cara mengurangi kelarutan dapat diamati pada saat air ditambahkan kedalam larutan phenolftalin, yakni munculnya larutan koloid yang berwarna putih seperti air susu.
Jelifikasi (gelatinasi)
Pada kondisi tertentu, sol dari berbagai koloid liofil dapat mengalami koagulasi dan berubah menjadi material dengan massa lebih rapat, disebut jeli. Prose pembentukan jeli seperti ini dinamakan jelifikasi atau gelatinasi.
Contoh dari proses ini misalnya pada pembuatan kue dan bahan agar-agar kanji atau silikagel.
Pembentukan jeli terjadi akibat mo;ekul-molekul senyawa berkoalisi membentuk rantai yang panjang. Jaringan rantai ini menyebabkan terbentuknya ruang-ruang kosong yang dapat diisi oleh cairan atau medium pendispersi, sehingga cairan tersebut terjebak dalam jaringan rantai.
Pembentukan jeli bergantung pada berbagai faktor, seperti suhu dan konsentrasi zat. Pada suhu tinggi agar-agar sukar mengeras dan akan memadat bila di dinginkan. Pembekuan jeli juga menuntut konsentrasi tinggi agar seluruh pelarut dapat terjebak dalam jaringan.
Kepadatan jeli bergantung pada zat terdispersi yang dikandungnya. Silikagel yang mengandung 94% – 97% air membentuk cairan kental seperti lendir. Bila kandungan airnya 90% – 92% akan lebih padat yang dapat dipotong dengan pisau.
Jika jeli dibiarkan, volumenya akan berkurang karena cairannya keluar. Gejala ini dapat diamati pada agar-agar yang dibiarkan lama. Gejala ini dinamakan sinersis. Jeli dapat dikeringkan hingga kerangkanya keras, dan pada akhirnya dapat membentuk kristal padat atau serbut. Jeli seperti ini mengandung banyak pori dan mempunyai kemampuan mengabsorpsi zat lain. Contohnya silikagel dapat digunakan sebagai pengering barang elektronik karena dapat menyerap air (bersifat higroskopis)