– Katalis secara sederhana adalah istilah terkait dengan zat kimia yang mempengaruhi laju reaksi kimia pada suhu tertentu dengan mengubah energi aktivasi yang diperlukan pada saat reaksi untuk diproses, Sedangkan katalisis secara sederhana adalah istilah terkait dengan proses yang terjadi akibat adanya peran dari katalis.
Katalis tidak dikonsumsi oleh reaksi dan dapat berpartisipasi dalam beberapa reaksi pada suatu waktu. Sedangkan katalisis secara sederhana adalah istilah terkait dengan proses yang terjadi akibat adanya peran dari katalis.
Katalis secara sederhana adalah istilah terkait dengan senyawa kimia yang dapat mempercepat reaksi tanpa perubahan bentuk/struktur dari katalis tersebut. Satu-satunya perbedaan antara reaksi dikatalisis dan reaksi yang tidak dikatalisis secara sederhana adalah istilah terkait dengan bahwa energi aktivasi berbeda. Tetapi tidak ada efek pada energi reaktan atau produk. ΔH untuk reaksi secara sederhana adalah istilah terkait dengan sama.
Katalis Positif dan Negatif
Biasanya ketika seseorang merujuk kepada katalis, yang artinya katalis positif, yaitu secara sederhana adalah istilah terkait dengan katalis yang mempercepat laju reaksi kimia dengan menurunkan energi aktivasi. Ada juga katalis negatif atau inhibitor, yang memperlambat laju reaksi kimia atau cendrung mengurangi terjadinya reaksi kimia.
Promotor dan Racun Katalitik
Promotor secara sederhana adalah istilah terkait dengan zat yang meningkatkan aktivitas katalis. Racun katalitik secara sederhana adalah istilah terkait dengan zat yang menonaktifkan katalis.
Bagaimana Katalis Kerja
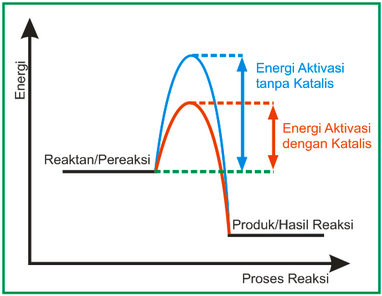
Katalis memungkinkan mekanisme alternatif untuk reaktan menjadi produk, dengan energi aktivasi yang lebih rendah dan dalam keadaan transisi yang berbeda.
Katalis memungkinkan reaksi berlangsung pada suhu yang lebih rendah atau meningkatkan laju reaksi atau selektivitas. Katalis sering bereaksi dengan pe-reaksi untuk membentuk zat perantara yang akhirnya menghasilkan produk reaksi yang sama dan meregenerasi katalis.
Perlu dicatat bahwa katalis dapat dikonsumsi selama langkah intermediet, tetapi akan dibuat lagi sebelum reaksi selesai.
Artikel lainnya:
- Jenis-jenis Energi Potensial dan Contohnya