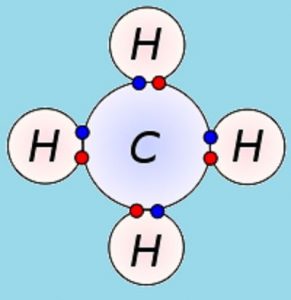
Karbon (dari bahasa Latin carbo, batubara) adalah unsur kimia yang lambangnya adalah C, massa atom 12 u, nomor atom 6 (6 elektron dan 6 proton) dan berbentuk padat pada suhu kamar.
Ini adalah anggota kelompok 14 dari tabel periodik, itu adalah non-logam dan tetravalen, memiliki empat elektron yang tersedia dalam bentuk ikatan kovalen.
Ada tiga isotop alami , 12C dan 13C menjadi isotop stabil, di mana 14C adalah radioaktif, perlahan meluruh dengan waktu paruh sekitar 5730 tahun. Ini adalah salah satu dari sedikit unsur kimia yang ditemukan sejak zaman kuno.
Pengertian
Karbon adalah salah satu unsur yang paling penting di Bumi dan membentuk dasar kimia kehidupan. Ini adalah lima belas unsur paling melimpah di kerak bumi dan unsur yang paling berlimpah keempat dalam seluruh alam semesta, dalam hal massa.
Karakteristik
- Simbol: C
- Massa Atom: 12 u
- Nomor atom: 6
- Titik lebur: 3550 °C
- Titik didih: 4289°C
- Bentuk alotropik: Intan dan grafit.
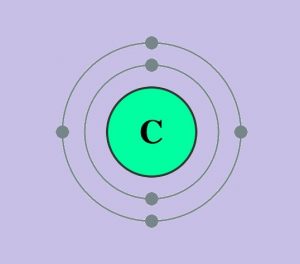
- Konfigurasi Elektronik: 1s², 2s², 2p²
- Hibridisasi: sp³
Karbon memiliki karakteristik penting: seperti semua materi di planet ini, ia tidak dapat diciptakan atau dihancurkan, sehingga jumlah karbon yang tersedia terbatas.
Fungsi
Karbon dapat bertindak di atmosfer sebagai agen utama untuk menyediakan panas dalam bentuk CO2 yang menghasilkan efek rumah kaca, juga sebagai agen utama fotosintesis tanaman dan, di samping itu, semua struktur organik menghasilkan karbon dalam struktur molekulnya.
Karbon membentuk kulit , kuku , daun , antara lain. Ketika suatu organisme mati, bahan ini dikembalikan ke lingkungan dan diserap kembali oleh organisme lain.
Hal ini terjadi karena mikroorganisme yang sangat bertanggung jawab untuk dekomposisi mengembalikan karbon ke atmosfer dalam bentuk karbon dioksida.
Aplikasi
Salah satu aplikasi industri karbon adalah sebagai komponen hidrokarbon , terutama dalam bahan bakar seperti minyak dan gas alam .
Yang pertama diperoleh dengan penyulingan di kilang bensin, sedangkan yang terakhir digunakan sebagai sumber energi berkat pembakarannya yang lebih bersih. Minyak tanah dan minyak digunakan sebagai bahan baku untuk mendapatkan plastik .
Baru-baru ini telah dianggap sebagai salah satu unsur utama untuk pengembangan elektronik molekuler atau molekuler.
Apakah yang dimaksud dengan Isotop?
Identitas suatu unsur kimia yang berbeda dibentuk oleh nomor atom yang unik. Nomor atom adalah jumlah proton dalam inti atom. Sifat lain adalah massa atom dari unsur, yang merupakan jumlah proton dan neutron dalam inti atau massa dari inti atom.
Inti dari unsur kimia yang sama mungkin memiliki nomor atom sama tetapi nomor massa atom yang berbeda. Inti semacam ini disebut isotop unsurnya. Karena, sifat-sifat kimia tergantung pada nomor atom, isotop ini secara kimiawi serupa, namun berbeda dalam sifat fisik tertentu.
Berapa Banyak Isotop Karbon yang Ada?
Hanya berapa banyak isotop karbon yang ada? Karbon memiliki sebanyak 15 isotop! Mereka semua memiliki nomor atom 6, namun berbeda dalam massa atom mereka. Meskipun mereka semua memiliki jumlah proton yang sama (6), masing-masing berbeda dalam jumlah neutron dalam inti. Kebanyakan dari mereka adalah radioaktif.
Radioaktivitas menunjukkan bahwa inti ini tidak stabil dan meluruh dengan memancarkan radiasi pengion. Berikut adalah daftar dari semua isotop, bersama dengan beberapa sifat mereka yang paling penting.
Yang merupakan Isotop karbon paling stabil?
Seperti yang Anda lihat pada tabel di atas, hampir semua kecuali tiga dari isotop karbon yang stabil dan ada untuk waktu yang sangat singkat, sebelum mereka meluruh. Dari 15, 13 adalah isotop radioaktif. Tiga yang paling stabil adalah C12, C13 dan C14. Ini juga merupakan isotop alami, sementara yang lain diciptakan melalui transmutasi unsur buatan. Dari ketiganya, C14 adalah radioaktif, sementara dua lainnya tidak. C12 adalah yang paling berlimpah di Bumi, merupakan sekitar 98,93% dari atom dalam satu mol karbon, C13 adalah sekitar 1,07% dan C14 adalah yang paling langka (1 bagian dalam triliun).
Isotop Isotop
Isotop karbon Digunakan Untuk apa?
Ada banyak penggunaan karbon. C12 menjadi yang paling melimpah dari tiga isotop karbon dan elemen ini menjadi tulang punggung kehidupan di Bumi, penggunaan karbon tidak terbatas. Semua proses metabolisme termasuk proses kehidupan mempertahankan respirasi dan fotosintesis, yang dimungkinkan oleh senyawa berbasis karbon. Bahan bakar fosil yang dibuat dari karbon berbasis bahan organik mati. Semua kebutuhan energi kita dipenuhi oleh karbon berbasis cadangan minyak mentah dan gas alam.
C13 memiliki aplikasi pada NMR (Nuclear Magnetic Resonance), karena memiliki spin nuklir, yang dapat merespon sinyal frekuensi radio (sebagai lawan C12 yang belum). Protein penentuan struktur menggunakan NMR dimungkinkan dengan label protein dengan atom C13. Dalam ilmu bumi, C13 digunakan untuk menentukan identitas sumber air dengan mempelajari rasio sehubungan dengan isotop karbon lainnya.
C14 adalah isotop radioaktif karbon yang terutama digunakan dalam teknik penanggalan radiokarbon. Dengan menggunakan teknik ini, para arkeolog dapat menentukan umur karbon yang mengandung bahan-bahan yang sudah tua hingga 60,00 tahun. Sebuah pengetahuan tentang waktu paruh dari C14, bersama dengan current ratio C12 ke C14, membantu dalam menentukan umur benda arkeologi.
Karbon adalah yang paling serbaguna dari semua unsur ketika Anda menganalisis jangkauan yang luas dari aplikasi di alam. Menjadi unsur yang paling berlimpah keempat dalam alam semesta, sebagian besar sistem galaksi dan sebagian besar bintang-bintang dengan sistem tenaga surya pasti akan memiliki kehidupan berbasis karbon, mirip dengan kehidupan berbasis di Bumi!